 打印
打印根据《兽药管理条例》、《兽药注册办法》及《动物病原微生物菌(毒)种保藏管理办法》等有关规定,制定兽药注册菌(毒、虫)种、细胞委托保藏流程。
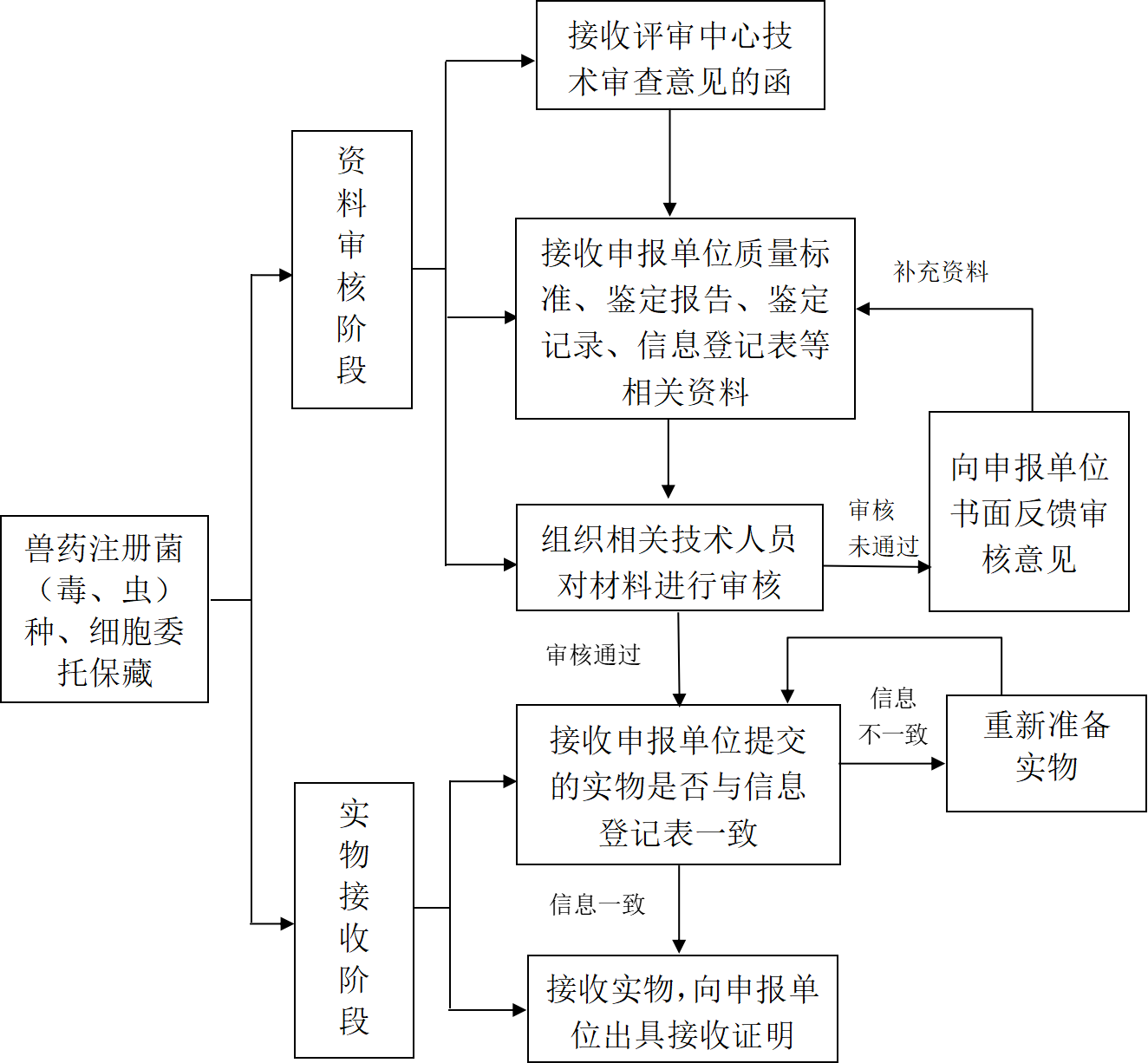
一、委托保藏流程
(一)资料审核阶段
1.接收评审中心技术审查意见的函。
2.接收申报单位提交的纸质资料并进行初步审核。
3.组织技术人员对纸质资料进行审核:审核通过,通知申报单位提交实物;审核未通过,向申报单位书面反馈审核意见。
4.资料审核时限一般约为10个工作日。
(二)实物接收阶段
检查申报单位提交的实物信息是否与信息登记表一致:信息一致,接收实物,向申报单位出具接收证明;信息不一致,告知申报单位并要求重新提交实物。
二、纸质资料要求及其注意事项
(一)农业农村部兽药评审中心“新兽药注册申报资料技术审查意见的函”以及工艺规程等附件复印件一份。
(二)菌(毒)种、细胞鉴定标准和全面鉴定报告一份。
1. 菌(毒)种、细胞鉴定标准和全面鉴定报告需提交加盖公章的原件,鉴定标准应与最终确定的工艺规程一致,鉴定报告中的鉴定项目应与标准顺序一致。
2. 菌(毒、虫)种、细胞的代次均应符合工艺规程中基础菌(毒、虫)种、细胞的代次要求。
(三)菌(毒)种、细胞鉴定原始记录复印件一份。
鉴定记录应与鉴定报告中的鉴定项目顺序一致,应包括详细的试验操作过程,涉及图表的应作适当标注并确保清晰。
(四)委托保藏菌(毒)种/细胞信息登记表一式两份。
1. 需经法定代表人或授权代表签字并加盖公章,若涉及多页内容,还需加盖骑缝章。所填内容需与提交的菌(毒、虫)种和细胞实物信息一致。
2. 需填写农业农村部兽药评审中心函号,并在对应的方框内打钩。
3. 制品名称栏请填写疫苗或诊断制品的名称,应与农业农村部兽药评审中心“新兽药注册申报资料技术审查意见的函”中的制品名称一致。
4. 信息登记表应包含工艺规程中涉及的所有菌(毒、虫)种和细胞,若申请免于提交,可在备注中注明原因。
5. “代次”应符合工艺规程中基础菌(毒、虫)种、细胞的代次要求。
6. “用途”应写明相关菌(毒、虫)种、细胞在注册产品“生产”“检验”中的具体用途。
7. “包装”是指分装菌(毒、虫)种、细胞的冻存管、安瓿或西林瓶等具体容器。
8. “保存条件”需与规程中的保存条件一致。
9. “实物标签”栏请填写或张贴包含实物标签所有信息内容的文字或图片。
10. “移交人及联系方式”“移交日期”部分请勿提前填写,由提交实物的人员于提交实物时手动填写。
(五)自然科技资源平台微生物菌种登记表一份。
仅菌(毒、虫)种需要填写,细胞可不填写,相关内容尽量填写即可,无需加盖公章。
(六)进口兽药注册,应同时提交所需纸质资料的外文原件和中文翻译件,还应提供相关菌(毒)种报关单或相关海关审批文件复印件一份。
三、实物资源要求
(一) 菌(毒)种、细胞的数量应符合要求,菌(毒、虫)种、细胞委托保藏应各提交5支。
(二) 菌(毒)种、细胞包装应完好,无破损、泄漏。
(三) 瓶签信息应完整、清晰,应与委托保藏菌(毒)种/细胞信息登记表一致。
(四) 提交高致病性菌(毒)种的,应使用符合要求的特定包装,并与一般菌(毒)种分开包装。应按要求办理运输相关的审批事项,获得批准文件,并在规定的时间内由两名专人运送至保藏中心。